Cái gọi là độ cứn ng cacbonat giới hạn (Hj) đề cập đến giá trị tới hạn mà tại đó CaCO₃ không kết tủa trong các điều kiện và nhiệt độ chất lượng nước cụ thể, trong đó CO₂ tự do không có hoặc ở mức tối thiểu. Thông thường, trong hệ thống nước làm mát, giá trị này dao động từ 2 đến 4,5 mg tương đương/L. Tuy nhiên, bằng cách thêm các chất ức chế axit và cặn, hệ thống nước làm mát có thể duy trì mức độ cứng cacbonat cao hơn. Bài viết này giải thích mối quan hệ giữa các chất ức chế quy mô cho nước làm mát và độ cứng cacbonat giới hạn, cung cấp thông tin hữu ích cho các chuyên gia xử lý nước.
1. Bổ sung axit và giới hạn độ cứng cacbonat
Bằng cách thêm axit vào nước trang điểm, độ cứng cacbonat được chuyển thành độ cứng không cacbonat với độ hòa tan cao hơn (chẳng hạn như CaSO₄ và CaCl₂), làm giảm độ cứng cacbonat của nước tuần hoàn xuống mức dưới độ cứng cacbonat giới hạn, do đó ngăn ngừa sự đóng cặn. Các phản ứng hóa học như sau:
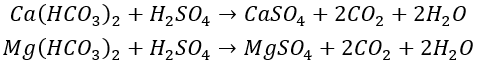
Tiếp tục chia sẻ phương pháp tính lượng axit cần thêm vào dựa trên độ cứng cacbonat và độ cứng cacbonat giới hạn (Hj), như thể hiện trong công thức sau.

Trong công thức:
G là lượng axit được thêm vào, kg/h;
E là khối lượng mol của axit, đối với axit sulfuric, E = 49, và đối với axit clohydric, E = 36,5;
Qm là thể tích nước bổ sung của nước làm mát tuần hoàn, m³/h;
α là nồng độ của axit;
HB là độ cứng cacbonat của nước bổ sung, mmol/L;
H′B là độ cứng cacbonat của nước bổ sung sau khi xử lý axit, mmol/L.
H′B có thể được tính như sau.
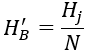
Trong công thức: N là bội số nồng độ; Hj là độ cứng cacbonat giới hạn của hệ thống nước làm mát tuần hoàn, tính bằng mmol/L.
Độ cứng cacbonat giới hạn của nước tuần hoàn sau khi thêm axit, không có chất ức chế cặn, có thể được tính bằng công thức sau:
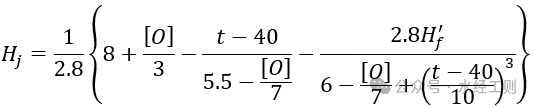
Trong công thức, [O] biểu thị mức tiêu thụ oxy, tính bằng mg/L; t biểu thị nhiệt độ của nước tuần hoàn, tính bằng ℃.
Hf′ là độ cứng không cacbonat sau khi xử lý với axit được thêm vào nước bổ sung, tính bằng mmol/L, và có thể được tính bằng công thức sau:
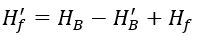
2. Sử dụng chất ức chế quy mô với xử lý axit để hạn chế độ cứng cacbonat
Khi sử dụng phương pháp xử lý bằng axit để hạn chế độ cứng cacbonat kết hợp với chất ức chế cặn, loại chất ức chế cặn được sử dụng phải xác định giá trị Hj thích hợp. Các chất ức chế vảy phổ biến bao gồm polyphosphate, phosphonate hữu cơ (muối) và axit polyacrylic.
Chất ức chế quy mô Polyphosphate
Polyphosphate chủ yếu đề cập đến natri polyphosphate, các dạng thường được sử dụng là natri hexametaphosphate (còn được gọi là natri polymetaphosphate) và natri tripolyphosphate. Những chất ức chế này phân tán và ổn định các hạt keo và có khả năng chelat hóa mạnh đối với các ion canxi và magie. Natri polyphosphate không chỉ có chức năng như một chất ức chế quy mô mà còn có đặc tính ức chế ăn mòn. Các đặc tính cụ thể khác nhau tùy thuộc vào cấu trúc phân tử của [NaPO₃] n , trong đó giá trị của n xác định các đặc tính. Natri hexametaphosphate có công thức hóa học [NaPO₃]₆ONa₂ và là một polyme của natri metaphosphate (NaPO₃). Khi được sử dụng làm chất ức chế cặn, độ cứng cacbonat giới hạn Hj của nước tuần hoàn có thể được ước tính bằng công thức sau. Liều lượng điển hình của natri hexametaphosphate dao động từ 1 đến 5 mg/L, với giới hạn trên được sử dụng cho nước có độ cứng cacbonat cao. Natri tripolyphosphate (Na₅P₃O₁₀) có khả năng chelat hóa các ion canxi mạnh, với liều lượng thông thường từ 2 đến 5 mg/L và Hj = 5 mmol/L.
Hạn chế của polyphosphate là xu hướng phân hủy thành orthophosphate trong nước, một quá trình được gọi là thủy phân polyphosphate. Mức độ thủy phân bị ảnh hưởng bởi các yếu tố như pH, nhiệt độ, thời gian và hoạt động của vi sinh vật. Quá trình thủy phân có mối tương quan thuận với nhiệt độ nước và thời gian tiếp xúc, mặc dù nó xảy ra với tốc độ tương đối chậm, với tốc độ thủy phân điển hình từ 11% đến 35%.
Phosphonat hữu cơ và muối của chúng
Những chất ức chế vảy này có hiệu quả và cũng có tác dụng ức chế ăn mòn, khiến chúng trở thành chất ức chế hai mục đích. Nhiều đặc tính của chúng tương tự như polyphosphate, nhưng chúng ổn định hơn và ít bị thủy phân hơn, ngay cả ở nhiệt độ cao hơn. Tuy nhiên, phosphonate hữu cơ có thể ăn mòn đồng, vì vậy chúng không thích hợp để sử dụng trong các hệ thống trao đổi nhiệt bằng đồng. Các phosphonate hữu cơ phổ biến và muối của chúng được sử dụng trong nước bao gồm axit hydroxyethylidene diphosphonic (HEDP), axit aminotrimethylene phosphonic (ATMP) và ethylenediaminetetra (axit methylenephosphonic) (EDTMP). Khi sử dụng cùng với polyphosphate, các chất ức chế này có thể có tác dụng hiệp đồng, cải thiện độ cứng cacbonat hạn chế của nước tuần hoàn và giảm liều lượng của từng chất. Độ cứng cacbonat giới hạn điển hình của các chất ức chế này như sau:
HEDP: Hj = 8 mmol/L
ATMP: Hj = 9 mmol/L
EDTMP: Hj = 8 mmol/L
Polyme polycarboxylat
Polyme polycarboxylate là các polyme chứa nhóm chức carboxyl (nhóm carboxyl) hoặc dẫn xuất của axit cacboxylic. Anion carboxylate (COO⁻) xác định các đặc tính của các polyme này, trong đó M đại diện cho một cation hóa trị một, hydro hoặc một nhóm amin. Sau khi được đưa vào nước, nhóm carboxylate phân ly thành COO⁻ và M⁺, trong đó COO⁻ chịu trách nhiệm ức chế cặn. Các chất ức chế quy mô polycarboxylate phổ biến được sử dụng trong nước bao gồm axit polyacrylic, natri polyacrylate, polymethyl methacrylate, copolyme của axit acrylic và hydroxypropyl acrylate, copolyme của axit acrylic và acrylat, và poly (axit maleic) thủy phân (anhydrit). Các liều lượng điển hình và các giá trị độ cứng cacbonat giới hạn tương ứng như sau:
Axit polyacrylic: 1–9 mg/L, Hj = 5,5–10 mmol/L
Natri polyacrylat: 1–8 mg/L, Hj = 5,8–9 mmol/L
Poly(axit maleic): 1–5 mg/L, Hj = 5–8,5 mmol/L
Tóm tắt
Bằng cách kiểm soát độ cứng cacbonat hạn chế trong hệ thống nước làm mát tuần hoàn, có thể ngăn chặn sự hình thành cặn. Sử dụng các phương pháp trên để tính toán liều lượng axit và chất ức chế cặn thích hợp, cùng với độ cứng cacbonat giới hạn cho phép của hệ thống trong các điều kiện vận hành cụ thể, giúp ngăn ngừa các vấn đề về cặn đồng thời giảm chi phí hóa chất.


